Diferença entre os elementos de bloco S e P | S vs P Elementos de bloco
Diferença-chave - S vs. P Elementos de Bloque
A diferença de chave entre elementos de bloco s e p pode ser melhor explicada usando sua configuração eletrônica. Nos elementos de bloqueio s, o último elétron enche o subshell e os elementos do bloco p, o último elétron se enche para a subshell p. Quando formam íons; Os elementos de bloqueio de s removem seus elétrons da subshell ultraperiférica facilmente, ao passo que os elementos de bloco p aceitam elétrons na subcascatura p ou removem elétrons do subconjunto p. Alguns elementos no grupo p formam íons positivos removendo elétrons do p-subshell externo e alguns elementos (os elementos mais eletronegativos) formam íons negativos aceitando um elétron de outros. Quando você considera as propriedades químicas, há uma diferença significativa entre os elementos do bloco s e p; Isto é basicamente devido à configuração eletrônica.
O que são os elementos do bloco S?
Os elementos do bloco S são os elementos químicos do grupo I e do grupo II na tabela periódica. Uma vez que o subshell da s pode acomodar apenas dois elétrons, esses elementos geralmente possuem um (grupo I) ou dois (grupo II) elétrons na casca mais externa. Os elementos dos grupos I e II são mostrados acima na tabela.
- diff Artigo Médio antes da Tabela ->| IA | II A | |
| 2 | Li | Be |
| 3 | Na | Mg |
| 4 | K | Ca |
| 5 | Rb | Sr |
| 6 | Cs | Ba |
| 7 | Fr | Ra |
| IA | Metais alcalinos |
| II A | Metais alcalino-terrosos |
Todos os elementos do bloco s formam íons positivos e são muito reativos.
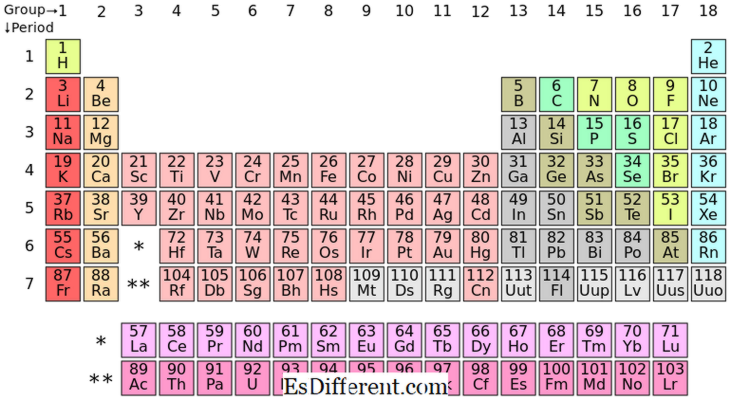
A colocação dos elementos do bloco S na tabela periódica
O que são os elementos P-block?
Os elementos do bloco P são os elementos cujo último elétron se enche de p subshell. Existem três p orbitais; cada orbital pode acomodar dois elétrons, fazendo o total de seis p-elétrons. Portanto, os elementos de bloco p têm um a seis p-elétrons na capa mais externa. O bloco P contém metais e não metais; Além disso, existem alguns metalóides também.
| 13 | 14 | 15 | 16 | 17 | 18 | |
| 2 | B | C | N | O | F Ne | 3 |
| Al | Si | P | S | Cl | Ar | 4 |
| Ga | Ge | Como | Se | Br | Kr | 5 |
| Em | Sn | Sb | Te | I | Xe | 6 |
| Tl | Pb Bi | Po | Em | Rn | Qual a diferença entre os elementos de bloqueio S e P? | Configuração de elétron comum: |
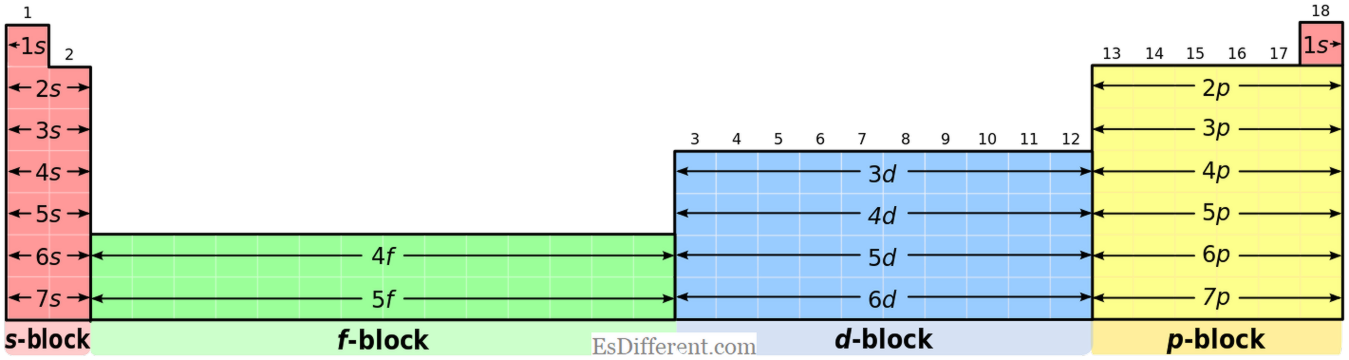
Elementos do bloco S:
Os elementos do bloco S possuem a configuração elétrica comum de [gás nobre] ns
1 (para elementos do grupo I) e [gás nobre] ns 2 (para elementos do grupo II). Elementos do bloco P: Os elementos do bloco P têm a configuração elétrica comum de [gás nobre] ns
2 np 1-6 . Mas, o hélio possui uma configuração 2 ; é uma situação especial. Estados de Oxidação: Elementos do bloco S:
Os elementos do bloco S não mostram múltiplos estados de oxidação como elementos do bloco p. Por exemplo, os elementos do grupo I mostram +1 o estado de oxidação e os elementos do grupo II mostram o estado de oxidação +2.
Elementos do bloco P: Ao contrário dos elementos do bloco s, os elementos de bloco p têm um estado de oxidação comum para o respectivo grupo na tabela periódica e alguns outros estados de oxidação adicionais dependendo da estabilidade do íon.
Grupo 13
| 14 | 15 | 16 | 17 | 18 | Configuração geral de elétrons | ns |
| 2 | np 1 ns 2 | np 2 ns 2 | np 3 ns 2 | np 4 ns 2 np | 5 ns 2 np | 6 1 st membro do grupo |
| Be < C N O | F | Ele | Número de oxidação comum | +3 | +4 | +5 |
| -2 | -1 | 0 | Outros estados de oxidação | +1 | +2, -4 | +3, -3 |
| +4, +2, | +3, +5, + 1, +7 | - | Propriedades: | Elementos do bloco S: | Em geral, todos os elementos do bloco s são metais. Eles são brilhantes, bons condutores elétricos e de calor e são fáceis de remover os elétrons da concha de valência. Eles são os elementos mais reativos na tabela periódica. | Elementos do bloco P: |
A maioria dos elementos do bloco p não são metais. Eles têm baixos pontos de ebulição, maus condutores e difíceis de remover elétrons do casco mais externo. Em vez disso, eles ganham elétrons. Alguns dos não-metais são sólidos (C, P, S, Se) à temperatura ambiente enquanto alguns são gases (Oxigênio, Nitrogênio). O brometo é um não-metal, e é um líquido à temperatura ambiente.
Além disso, p-block contém alguns elementos metálicos; alumínio (Al), gálio (Ga), índio (In), estanho (Sn), talio (Tl), chumbo (Pb) e bismuto (Bi). Cortesia da imagem:
1. "Tabela periódica (poliatômica)" de DePiep [CC BY-SA 3. 0] via Commons 2. "Tabela periódica bloqueia spdf (32 column)" pelo Usuário: DePiep [CC BY-SA 3. 0] via Commons




