Diferença entre acetaldeído e acetona | Acetaldehyde vs Acetone
Diferença-chave - Acetaldeído versus acetona
Tanto o acetaldeído como a acetona são pequenas moléculas orgânicas, mas há uma diferença entre elas com base em seus grupos funcionais. Em outras palavras, eles são dois compostos de carbonilo diferentes com diferentes propriedades químicas e físicas. A acetona é o membro mais pequeno do grupo cetona, enquanto o acetaldeído é o menor membro do grupo aldeído. A diferença-chave entre o acetaldeído e a acetona é o número de átomos de carbono na estrutura; acetona tem três átomos de carbono , mas acetaldeído tem apenas dois átomos de carbono. A diferença no número de átomos de carbono e com dois grupos funcionais diferentes leva a muitas outras diferenças em suas propriedades.
O que é a acetona?
A acetona é o membro mais pequeno do grupo cetona, também conhecido como propanona . É um líquido incolor, volátil e inflamável que é usado como solvente. A maioria dos solventes orgânicos não se dissolve em água, mas a acetona é miscível com água. É muito frequentemente usado para fins de limpeza no laboratório e como o principal ingrediente ativo em líquidos removedores de esmaltes e em diluente de tinta.

O que é o acetaldeído?
O acetaldeído, também conhecido como etanal é o menor membro do grupo aldeído. É um líquido incolor e inflamável com forte cheiro sufocante. Existem muitos usos industriais, como a produção de ácido acético, perfumes, drogas e alguns sabores.
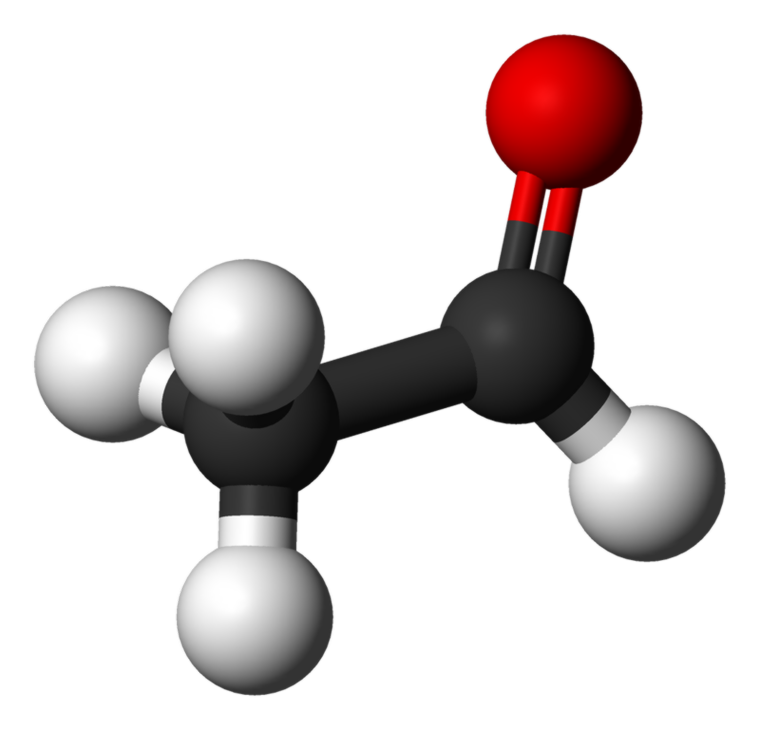
Qual a diferença entre o acetaldeído e a acetona?
Estrutura e Propriedades Gerais de Acetaldeído e Acetona
Acetona: A fórmula molecular da acetona C 3 H 6 O. É o membro mais simples da família cetona. É um líquido volátil e inflamável com um odor pungente.

Acetaldeído: A fórmula molecular do acetaldeído C 2 H 4 O. É o mais simples e um dos membros mais importantes da família de aldeídos. É um líquido incolor, volátil e inflamável à temperatura ambiente.

Ocorrência de acetaldeído e acetona
Acetona: Em geral, a acetona está presente no sangue humano e na urina. Também é gerado e descartado no corpo humano durante o metabolismo normal. Quando as pessoas têm diabéticos, elas são produzidas em maiores quantidades no corpo humano.
Acetaldeído: O acetaldeído é naturalmente encontrado em várias plantas (café), pão, vegetais e frutas maduras.Além disso, é encontrado na fumaça de cigarro, gasolina e escape de diesel. Além disso, é um intermediário no metabolismo do álcool.
Usos de acetaldeído e acetona
Acetona: A acetona é usada principalmente como solvente orgânico nos laboratórios químicos e também é o agente ativo na produção de removedor de esmalte e diluente na indústria de tintas.
Acetaldeído: A acetona é usada para fabricar ácido acético, perfumes, corantes, agentes aromatizantes e medicamentos.
Características do acetaldeído e da acetona
Identificação
Acetona: A acetona dá um resultado positivo para o teste de iodoforo. Portanto, pode ser facilmente diferenciado do acetaldeído usando teste de iodoform.
Acetaldeído: O acetaldeído dá um espelho de prata ao "Reagente de Tollen" enquanto que as cetonas não dão um resultado positivo para este teste. Porque, não pode se oxidar facilmente. O teste de ácido cromático e o reagente de Fehling também podem ser usados para identificar o acetaldeído.
Reatividade
A reactividade dos grupos carbonilo (aldeídos e cetonas) deve-se principalmente ao grupo carbonilo (C = O).
Acetona: Geralmente, os grupos alquilo são grupos de doação de elétrons. A acetona possui dois grupos metilo e diminui a polarização do grupo carbonilo. Por isso, torna o composto menos reativo. Dois grupos de metilo unidos aos dois lados do grupo carbonilo levam a um obstáculo mais esteárico também. Portanto, a acetona é menos reativa do que o acetaldeído.
Acetaldeído: Em contraste, o acetaldeído possui apenas um grupo metilo e um átomo de hidrogênio ligado ao grupo carbonilo. À medida que o grupo metilo doa elétrons, o átomo de hidrogênio retira os elétrons; Isso torna a molécula mais polarizada e torna a molécula mais reativa. Em comparação com a acetona, o acetaldeído tem menos efeitos esteáricos e outras moléculas podem se aproximar facilmente. Devido a estas razões, o acetaldeído é mais reativo do que a acetona.



